- Главная
- / Научные работы
- / Ушаков Сергей
- Методы отбора проб крови
Методы отбора проб крови
Сергей Ушаков, кандидат ветеринарных наук, технолог ЗАО «Консул»
Кровь – жидкая ткань организма, выполняющая ряд функций, одной из которых является транспортная. Осуществляя в организме транспорт химических веществ, происходит интеграция биохимических процессов в различных клетках и межклеточных пространствах в единую систему. Правильно отобранные образцы крови предоставляют возможность мониторинга нозологического профиля поголовья, уровня метаболических процессов, обеспеченности организма витаминами, минералами, незаменимыми аминокислотами и т.д. Для получения достоверных результатов необходимо свести к минимуму возможность появления артефактов, обусловленного нарушением правил отбора проб крови, ее стабилизирования и транспортировки.
Иглы перед взятием крови от каждого животного обязательно стерилизуют кипячением, либо применяют стерильные. Оптимальным вариантом является использование шприц-пробирок или вакуумных пробирок. При их использовании кровь не контактирует с внешней средой, т.е. остается асептической и не подвергается окислению кислородом воздуха, тем самым предупреждается агрегация тромбоцитов и образование сгустков в образцах, предназначенных для полного определения клеточного состава крови. Место пункции необходимо обработать 70%-ным спиртовым раствором или 3%-ным раствором карболовой кислоты. При заборе крови нужно следить, чтобы она стекала по стенке в пробирку струей, а не каплями. Кровь, взятая каплями и вспененная, быстрее гемолизируется и часто дает неправильные результаты показаний при лабораторных исследованиях.
Таблица 1. Влияние гемолиза на результаты исследований биохимических компонентов сыворотки крови
Существует несколько способов отбора проб крови у свиней. Среди них можно выделить:
- Из ушной вены и вены хвоста
Данный способ подходит, если необходимо отобрать небольшое количество крови (2-3 мл). Для асептического отбора используется шприц с иглой толщиной 0,8 мм (типа Луер), и отбор крови осуществляется при внутривенном введении иглы, в противном случае происходит бакобсемененность образца. Вены уха свиньи, как правило, расположены в трех точках уха и легко различимы. Одна вена располагается вдоль внешнего края уха, другая – посередине, третья – около 2 см от медиального края. Хвостовые вены находятся в вентральной части хвоста. Для этого способа взятия крови требуются иглы 0,8х25 мм.
После отбора крови необходимо удалить иглу, а место пункции пережать лещеткой, лигатурой или большим пальцем руки на 2-3 минуты. Опасность метода состоит в том, что лигатура может произвольно соскочить и произойдет обескровливание организма животного.
- Из яремной вены
Это безопасный и быстрый способ отбора крови, требующий правильной фиксации животного. Для этого используют металлическую петлю или веревку, при помощи которых животное фиксируется в стоячем положении. При фиксации голова поросенка должна быть поднята вверх таким образом, чтобы шея образовала прямую линию, а кожа была натянута.
Отбор крови производят с правой стороны (при дыхательной недостаточности, развивающейся у свиней при пневмонии или плевропневмонии возможно при введении иглы повреждение левого диафрагмального или блуждающего нерва, поэтому рекомендуется введение иглы справа). Точка пункции находится на краю плечеголовной мышцы – внешнего края яремного желоба, на линии между краем плечевого сустава и рукояти грудной кости (рис 1, 2). Вторая линия проходит от рукояти грудной кости к основанию уха. Глубина прокола для взрослых животных составляет от 75 до 100 мм, для маленьких поросят – 40-75 мм.
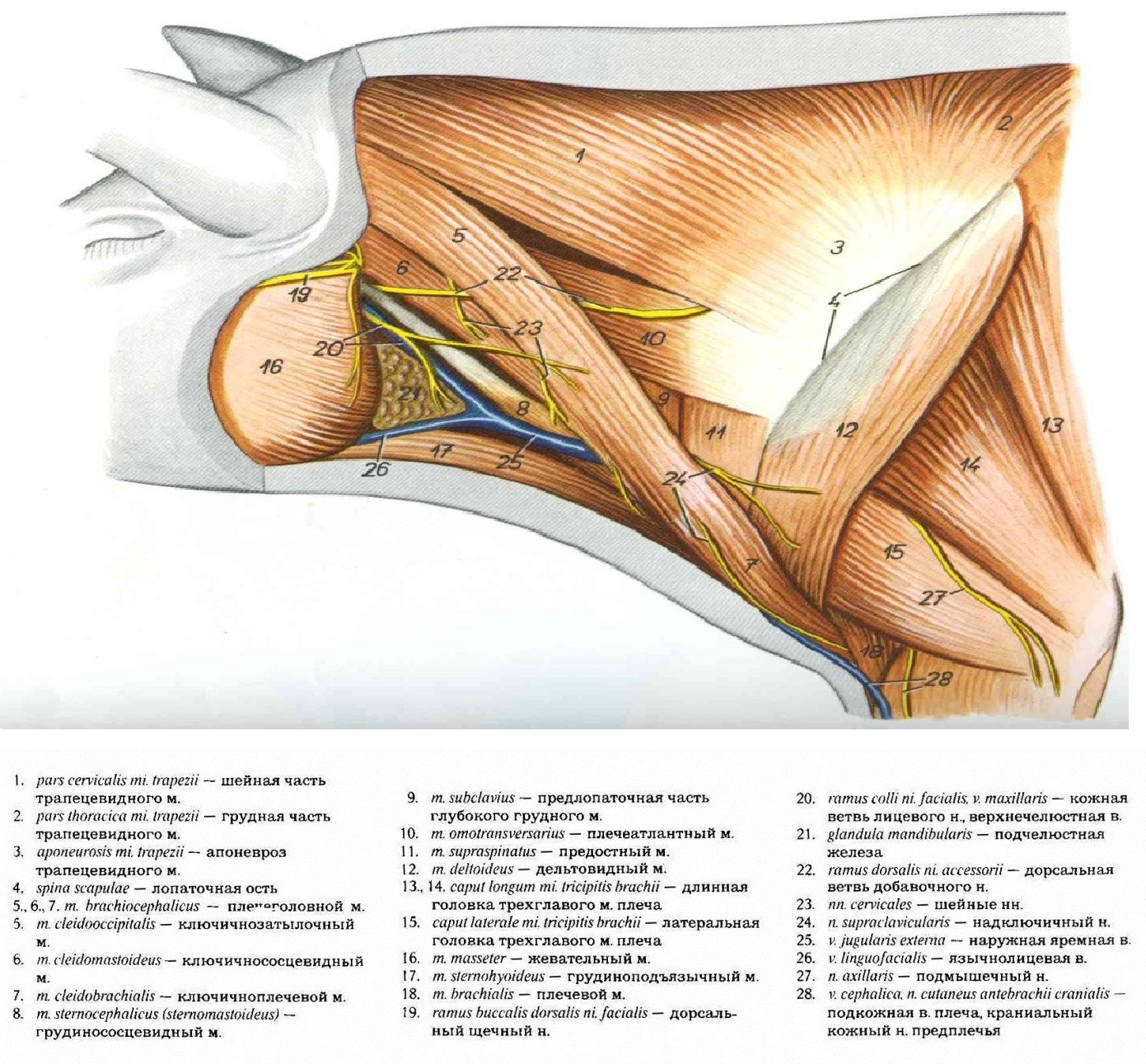
Рис. 1. Поверхностные мышцы шеи свиньи
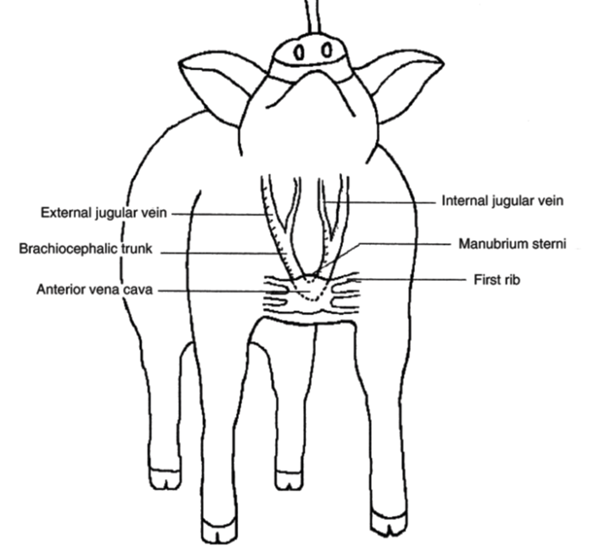
Рис. 1.1. Сеть венозных сосудов шеи

Рис. 2. Место пункции яремной вены
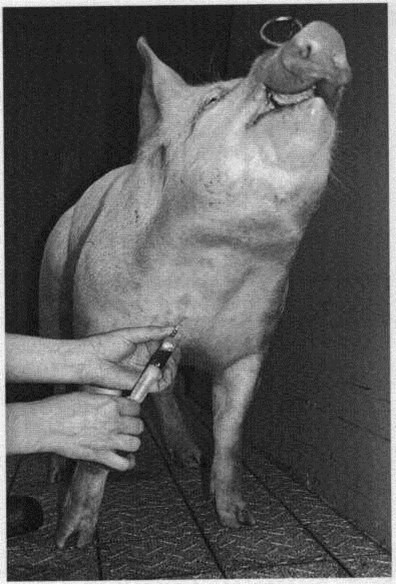
Рис. 3. Забор крови из яремной вены
После введения иглы под кожу поршень шприц-пробирки необходимо отвести назад для создания в ней отрицательного давления. Игла вводится в дорсомедиакаудальном направлении (рис. 3). Когда кровь начинает поступать в пробирку, необходимо следить, чтобы она не вспенивалась, не капала, не билась о дно, а плавно стекала по стенке – с целью предупреждения гемолиза эритроцитов.
Если игла с первого раза не попала в яремную вену, ее необходимо отвести назад и вводить в слегка измененном произвольном направлении. Если и в этот раз цель не достигается, иглу необходимо заменить. При наличии кровотечения после извлечения иглы, место пункции необходимо прижать большим пальцем руки до ее полной остановки.
- Из краниальной полой вены
Свиней массой <20 кг фиксируют в спинном лежачем положении, передние конечности фиксируются вдоль туловища, а голова вытягивается вперед (рис 4).
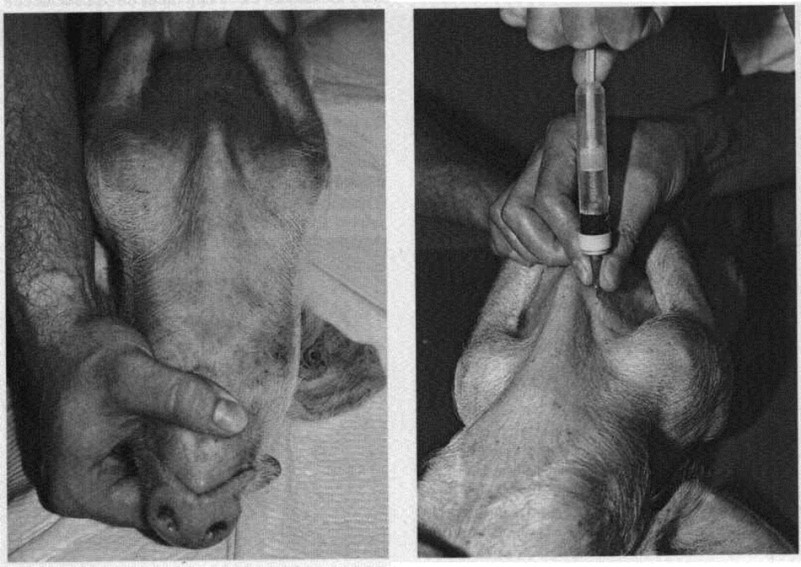
Рис. 4. Забор крови из краниальной полой вены
Для маленьких поросят требуется игла 0,8х40 мм, для взрослой свиньи – 1,2х100 мм. Точка пункции находится вблизи рукояти грудной кости в области первого ребра. Игла должна вводиться медленно вниз перпендикулярно телу между двумя первыми ребрами. Шприц вводится с небольшим вакуумом, как игла достигает полой вены, кровь будет поступать в шприц. Если кровь не поступает после первого введения, игла должна быть отведена назад и перенаправлена. Выводить иглу из полой вены необходимо, создав предварительно отрицательное давление.
Данный способ забора крови используется крайне редко ввиду возможных осложнений: гемоторракс, тампонада сердца, дыхательная недостаточность, прокол сонной артерии. Как правило, наблюдается до 10% отхода поросят, у которых кровь берется из краниальной полой вены. Поэтому более предпочтительным способом является забор из яремной вены.
- Орбитального венозного синуса
Техника взятия крови складывается с фиксации животного: маленьких поросят фиксируют в лежачем брюшном или спинном положении, взрослых свиней фиксируют петлей за верхнюю челюсть и привязывают к станку. Игла вводится до упора со стороны внутреннего угла глаза, через третье веко по направлению к противоположному локтевому бугру. Затем иглу отводят немного назад, и кровь набирается в шприц или пробирку. У взрослых свиней орбитальный синус немного смещается книзу, что необходимо учитывать при введении иглы. Если после введения иглы кровь не идет в течение 5-7 секунд, ее необходимо поменять на новую.
В некоторых случаях попадаются стресс-восприимчивые животные, это проявляется агрессией, сильно выраженными оборонительными действиями и усиленным визгом. В таком случае животное необходимо отпустить, обливать холодной водой на протяжении 10 мин и изолировать до прихода в нормальное состояние.
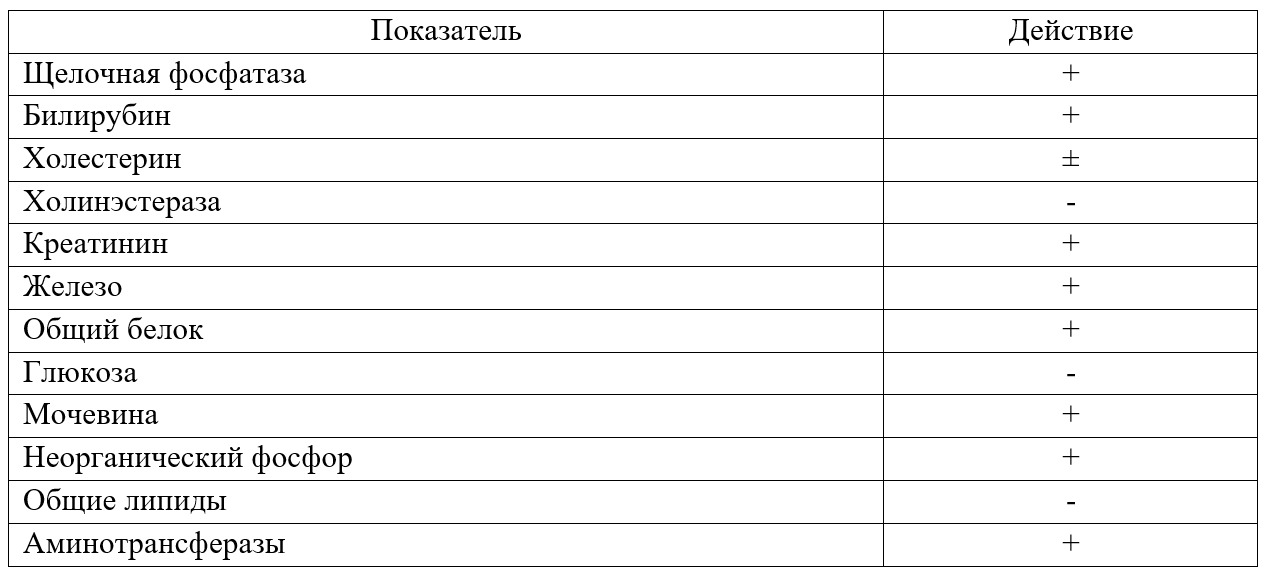
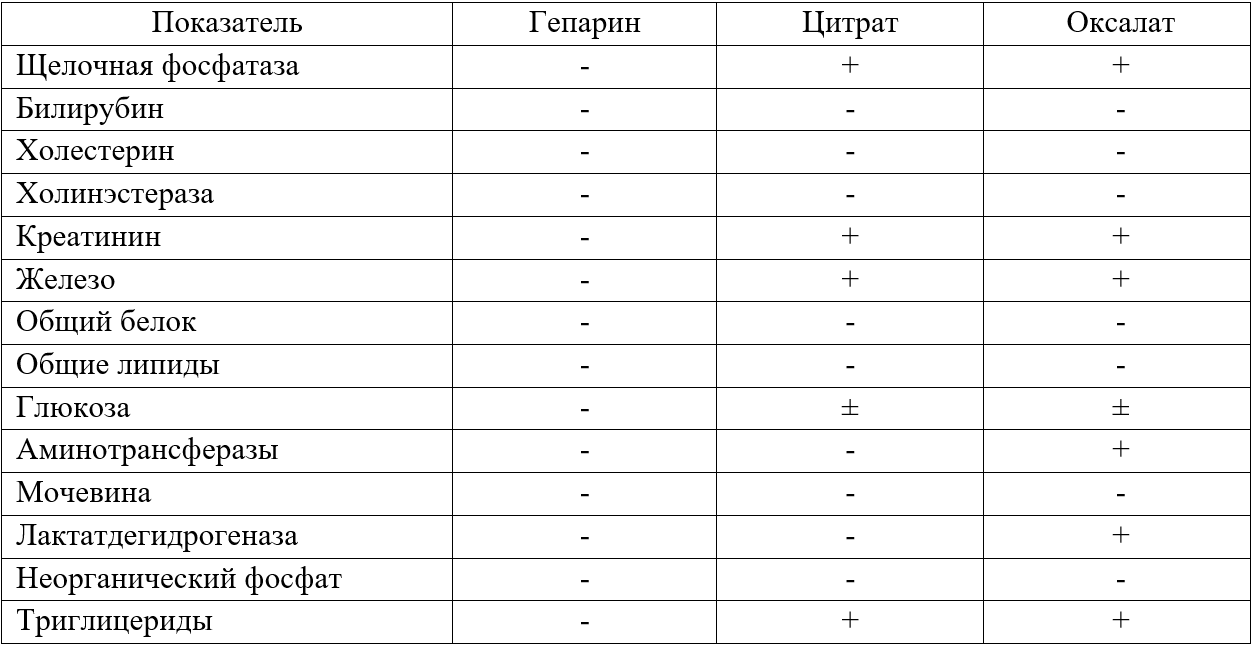
Для стабилизации крови можно использовать гепарин, цитрат натрия, ЭДТА и т.д. Лучше всего подходит ЭДТА и гепарин. Недостаток гепарина состоит в том, что в его присутствии лейкоциты окрашиваются хуже (предположительно вследствие связывания гепарина с клетками крови) и агрегация тромбоцитов сильнее, чем в случае применения ЭДТА. Необходимо также учитывать влияние антикоагулянта на биохимические (при биохимическом анализе плазмы крови) и общие клинические показатели крови (Табл. 2).
Таблица 2. Влияние антикоагулянтов на биохимические показатели крови
Брать кровь необходимо по возможности утром, до кормления животных. Голодание в течение ночи у животных с однокамерным желудком предотвращает возникновение липемии, которая может затруднить определение белков плазмы, фибриногена и гемоглобина. Примерно 25,4% ошибочных результатов при лабораторной диагностике связаны с несоблюдением правил отбора проб, 46% – хранения и транспортировки и 28,6% приходится на внутрилабораторные ошибки.
Для получения наиболее достоверных результатов пробы крови необходимо отправлять в лабораторию свежие (хранение неразделенной крови не более 2-х часов). При невозможности выполнить это требование необходимо как можно скорее отделить сыворотку от форменных элементов (в течение 1-2 часов), поскольку большинство ферментов (аланинаминотрансфераза, аспартатаминотрансферата, лактатдегидрогеназа, щелочная фосфатаза), а также калий, фосфор, медь - в высоких концентрациях содержатся в форменных элементах и диффундируют в сыворотку. Поэтому хранение неразделенной сыворотки и гемолиз приводят к высвобождению этих ферментов в сыворотку из клеток крови и завышению отдельных биохимических параметров. Глюкоза в этом случае наоборот убывает примерно на 10% в час за счет гликолитических процессов, протекающих в эритроцитах, а также убывает концентрация хлоридов, которые накапливаются в эритроцитах.
Транспортировать отделенную сыворотку в лабораторию при условии, что она будет исследована на следующий день, необходимо в термобоксе, при температуре 4-8оС, исключая воздействие света и тепла. Если сыворотка будет исследована позже, в течение недели или на следующей неделе, ее необходимо заморозить при -20оС и исследовать сразу же после разморозки.
Таким образом, если целью отбора крови является получение достоверных результатов, необходимо четко следовать методическим требованиям при отборе, хранении и транспортировке проб. В современных условиях (насыщенности ветеринарной программы, удаленности лаборатории от производства, отсутствия необходимого инвентаря и оборудования) этого сделать практически невозможно. Поэтому при интерпретации полученных из лаборатории результатов, необходимо учитывать все факторы, которые могут на них повлиять. Четкой границы, дифференцирующей патологию от физиологической нормы, у свиней не существует. На полученные из лаборатории результаты можно ориентироваться, но 100% им доверять нельзя.
Литературные источники
- Ветеринарная клиническая патология/ Джексон М. – 384 с.
- Мейер, Д. Ветеринарная лабораторная медицина. Интерпритация и диагностика /Д. Мейер, Дж. Харви // Перевод с англ. – М.: Софион, 2007. – 456 с.
- Schweinekrankheiten / K. Heinritzi, H.R. Gindele, G. Reiner, U. Schnurrbusch / Verlag eugen ulmer Stutgart. – 2006. – 480 p.
- Swine Nutrition Guide: 2 nd / Y.F. Patience et all. – 2001. – 271 p.
